化学の科学は非常に興味深いものであり、その知識はあらゆる人の人生に役立ちます。 しかし、特に教師が生徒のすべての質問に答える時間が必ずしもあるわけではないという事実を考慮すると、学校の教科書でそれを学ぶことはそれほど簡単ではないことがわかります。 E. N. フレンケルによって編纂されたこの自己啓発本は、まさにこの中ですべての質問に対する答えを見つけるために作成されました。
この本の情報は、できる限り理解できるように提示されています。 ここには乾いた事実だけが存在するわけではありません。 理論的な記述を読んで、通常の教科書には載っていない説明をすぐに見ることができます。 この本では、問題の解決方法も説明し、内容を強化するためのタスクを提供し、統一州試験で出題されるタスクも含まれています。 この本は、より深く理解したい人にとって役立ちます 通学コース化学、知識を深め、以前に学んだことを思い出してください。 学生や受験生が医科大学や化学科の試験の準備をする際に使用できます。 単に化学に興味があるが、何らかの理由で学校で化学に十分な注意を払わなかった人にとっても興味深いでしょう。 この本を読んだ後、化学はそれほど複雑ではなく、そして最も重要なことに、それは興味深い科学であることが理解できるようになります。
この作品は教育文学のジャンルに属します。 2016年にAST Publishing Houseから出版されました。 この本は「中学・高校。最高の指導法」シリーズの一部です。 私たちのウェブサイトでは、書籍「化学。独学マニュアル。試験に合格したいだけでなく、化学を理解し、化学を愛する人のための本。一般、無機および有機化学の要素」を fb2、rtf、epub、形式でダウンロードできます。 pdf、txt 形式、またはオンラインで読むことができます。 この本の評価は 5 点中 4.46 です。ここでは、読む前に、すでにこの本をよく知っている読者のレビューに目を向けて、意見を知ることもできます。 弊社のパートナーのオンライン ストアでは、この書籍を紙版で購入して読むことができます。
第1章。
一般的な化学的および環境的パターン。
化学はどこから始まるのでしょうか?
これは難しい質問ですか? 誰もが異なる答えをするでしょう。
中等学校では、学生は何年にもわたって化学を学びます。 多くの人は化学の最終試験で非常に良い成績を収めます。 しかし…
志願者や当時の 1 年生との会話によると、中等教育後に化学に関する知識が残っているのは重要ではありません。 さまざまな定義や化学式に混乱する人もいれば、生態学の概念や法則はおろか、化学の基本的な概念や法則すら再現できない人もいます。
彼らの化学反応は決して始まったわけではありません。
化学は、明らかに、その基礎、そして何よりも基本的な概念と法則を深く習得することから始まります。
1.1. 基本的な化学概念。
D.I.メンデレーエフの表では、元素記号の横に数字があります。 1 つの数字は元素の原子番号を示し、2 番目は原子質量を示します。 シリアル番号には独自の物理的な意味があります。 これについては後ほど説明しますが、ここでは原子量に焦点を当て、それがどのような単位で測定されるかを強調します。
表に示されている元素の原子量は相対値であることにすぐに注意してください。 相対原子質量の単位は、質量数 12 の同位体である炭素原子の質量の 1/12 とみなされ、原子質量単位 /amu/ と呼ばれます。 したがって、1アム 炭素同位体 12 C の質量の 1/12 に相当します。また、1.667 * 10 -27 kg に相当します。 /炭素原子の絶対質量は 1.99 * 10 -26 kg です。/
原子質量表に示されている は、原子質量単位で表される原子の質量です。 量は無次元です。 具体的には、各元素について、原子質量は、特定の原子の質量が炭素原子の質量の 1/12 より何倍大きいか小さいかを示します。
分子量についても同様のことが言えます。
分子量原子質量単位で表される分子の質量です。 大きさも相対的なものです。 特定の物質の分子量は、その分子を構成するすべての元素の原子の質量の合計に等しくなります。
化学における重要な概念は「モル」の概念です。 モル– 6.02 * 10 23 個の構造単位/原子、分子、イオン、電子など/を含む物質の量。 原子のモル、分子のモル、イオンのモルなど。
特定の物質の 1 モルの質量は、そのモル / またはモル / 質量と呼ばれます。 それは g/mol または kg/mol で測定され、文字「M」で示されます。 たとえば、硫酸のモル質量 M H 2 SO4 = 98 g/mol。
次の概念は「等価」です。 同等/E/ は、化学反応において 1 モルの水素原子と相互作用する、またはそのような量を置換する物質の重量です。 したがって、水素 E H の当量は 1 に等しくなります。 /E N =1/。 酸素当量 E O は 8 /E O =8/ に等しい。
元素の化学的等価物と複合物質の化学的等価物は区別されます。
要素に相当するものは可変量です。 それは、特定の化合物内でその元素が持つ原子量 /A/ と原子価 /B/ に依存します。 E=A/B。 たとえば、酸化物 SO 2 と SO 3 の硫黄当量を求めてみましょう。 SO 2 E S =32/4=8、SO 3 E S =32/6=5.33である。
グラム単位で表される当量のモル質量は当量質量と呼ばれます。 したがって、水素の当量質量 ME H = 1 g/mol、酸素の当量質量 ME O = 8 g/mol となります。
複合物質/酸、水酸化物、塩、酸化物/の化学当量は、1 モルの水素原子と相互作用する対応する物質の量です。 1当量の水素と置き換えたり、その量の水素や化学反応中の他の物質を置き換えたりすることができます。
酸当量/E K/ は、酸の分子量を反応に関与する水素原子の数で割った商に等しい。 酸 H 2 SO 4 の場合、両方の水素原子が H 2 SO 4 +2NaOH=Na 2 SO+2H 2 O と反応すると、当量は EN 2 SO4 = M H 2 SO 4 /n H =98/2=49 に等しくなります。
水酸化物当量/E ヒドロ。 /は、水酸化物の分子量を反応するヒドロキソ基の数で割った商として定義されます。 たとえば、NaOH の当量は次と等しくなります: E NaOH = M NaOH / n OH = 40/1 = 40。
食塩相当量/E 塩/ は、その分子量を、反応する金属原子の数とその価数の積で割ることによって計算できます。 したがって、塩 Al 2 (SO 4) 3 の当量は、E Al 2 (SO 4) 3 = M Al 2 (SO 4) 3 /6 = 342/2.3 = 342/6 = 57 に等しくなります。
酸化物当量/E ok / は、対応する元素と酸素の当量の合計として定義できます。 たとえば、CO 2 の当量は炭素と酸素の当量の合計に等しくなります: E CO 2 = E C + E O = 3 + 8 = 7。
気体物質の場合は、等価体積 /E V / を使用すると便利です。 通常の状態では、気体 1 モルは 22.4 リットルの体積を占めるため、この値に基づいて気体の等価体積を求めるのは簡単です。 水素について考えてみましょう。 水素のモル質量2gは22.4リットルの体積を占め、その等価質量1gは11.2リットル/または11200ml/の体積を占めます。 したがって、E V N =11.2lとなる。 塩素の等価体積は 11.2 l/E VCl = 11.2 l/です。 CO の等価体積は 3.56 /E V O =3.56 l/ です。
元素または錯体物質の化学当量は交換反応の化学量論的計算に使用され、酸化還元反応の対応する計算では酸化当量および還元当量が使用されます。
酸化当量は、酸化剤の分子量を、特定の酸化還元反応で受け取る電子の数で割った商として定義されます。
還元当量は、還元剤の分子量を所定の反応で放出する電子の数で割ったものに等しい。
酸化還元反応を書いて、酸化剤と還元剤の当量を決定してみましょう。
5N 2 asS+2KMnO 4 +8H 2 SO 4 =S+2MnSO 4 +K 2 SO 4 +5Na 2 SO 4 +8H 2 O
この反応における酸化剤は過マンガン酸カリウムです。 酸化剤の当量は、KMnO 4 の質量を反応において酸化剤が受け取る電子の数で割ったものに等しくなります(ne=5)。 E KMnO 4 =M KMnO 4 /ne=158/5=31.5。 酸性媒体中の酸化剤KMnO 4 の等量のモル質量は31.5 g/molである。
還元剤 Na 2 S の当量は、E Na 4 S = M Na 4 S / ne = 78/2 = 39 となります。 Na 2 S 相当のモル質量は 39 g/mol です。
エレクトロでは 化学プロセス特に物質の電気分解中には、電気化学的等価物が使用されます。 電気化学当量は、電極で放出された物質の化学当量をファラデー数 /F/ で割った商として求められます。 電気化学的等価物については、コースの対応する段落で詳しく説明します。
ヴァランス。 原子が相互作用すると、それらの間に化学結合が形成されます。 各原子は特定の数の結合しか形成できません。 結合の数によって、原子価と呼ばれる各元素の固有の特性が決まります。 最も一般的な形式では、原子価は化学結合を形成する原子の能力を指します。 水素原子が形成できる 1 つの化学結合が価数の単位と見なされます。 この点で、水素は 1 価の元素であり、酸素は 2 価の元素です。 酸素原子と結合を形成できる水素は 2 つまでです。
化合物を含む各元素の価数を決定できる能力は、化学コースを首尾よくマスターするために必要な条件です。
原子価は、次のような化学の概念にも関連しています。 酸化状態。 酸化基質とは、元素がイオン性化合物内に持つ電荷、または共有電子対がより電気陰性度の高い元素に完全にシフトした場合に共有結合性化合物内に持つであろう電荷です。 酸化状態には数値表現だけでなく、対応する電荷記号 (+) または (-) もあります。 ヴァランスにはこれらの兆候はありません。 たとえば、H 2 SO 4 の酸化状態は水素 +1、酸素 -2、硫黄 +6 であり、したがって価数は 1、2、6 になります。
数値上の価数と酸化状態は必ずしも値が一致するとは限りません。 たとえば、エチル アルコール CH 3 –CH 2 –OH の分子では、炭素の価数は 6、水素は 1、酸素は 2 で、たとえば最初の炭素の酸化状態は -3、2 番目の炭素は -3 です。 –1: –3 CH 3 – –1 CH 2 –OH。
1.2. 環境に関する基本的な概念。
最近、「エコロジー」という概念が私たちの意識に深く浸透しています。 この概念は 1869 年に E. ヘッケルによって導入され、ギリシャ語に由来しています。 オイコス- 家、場所、住居、 ロゴ– その教えは / 人類をますます混乱させています。
生物学の教科書では 生態学生物とその環境の間の関係の科学として定義されます。 エコロジーのほぼ一致した定義は、B. ネーベルの著書『環境の科学』の中で与えられています。エコロジーは、生物同士、および環境との相互作用のさまざまな側面の科学です。 より広範な解釈は他の情報源で見つけることができます。 たとえば、「エコロジー – 1/」です。 生物とその体系的な集合体、および環境の間の関係を研究する科学。 2/。 高分子から生物圏に至るまでの全身的な生物学的構造と、それ自体の間および環境との関係を研究する一連の科学分野。 3/。 勉強する規律 一般法さまざまな階層レベルでの生態系の機能。 4/。 生物の生息環境を研究する総合科学。 5/。 地球の生物圏における種としての人間の位置、生態系との関係、およびそれらへの影響についての研究。 6/。 環境生存の科学。 / N.A. アジジャニャン、V.I. 人間の生態。/. しかし、「エコロジー」という用語は、科学としての生態学だけを指すのではなく、環境そのものの状態とそれが人間、動植物に及ぼす影響を指します。
登録やSMSなしの無料オンラインスロットマシン Novomatic や Igrosoft など、最高のゲーム ソフトウェア開発者の 1 つになりました。 すべてのスロット マシンは、 フリーゲーム, 経験を積んだ経験豊富なユーザー向けでもあります。 提供されているゲームに興味がある場合は、賭けをした後に自動的にトリガーされるスーパー ボーナス ゲームが提供されます。 登録後、カジノ管理者に情報を提供する必要があります。 ただし、仮想クラブでは誰もが無料でプレイできることを忘れないでください。 お金のために遊びたい人はほとんどいません。
ただし、デモ モードについては忘れないでください。これは大きなリスクです。 サイト訪問についての率直な書面による声明。
支払いのルールと条件を明確にする前に、システムの要件。
思い出は、キーボードから始まり、ローンの形で法的資源となる可能性も含めて、重要な役割を果たします。 クレジットがなくなり、潜在意識の中での賭けが成就しました。
可能な限り安全な賭けでプレイすることを試みることもできます。
セキュリティを利用すると以下のような教育が受けられます。 インターネット上で最高のオンラインカジノへようこそ! 登録やSMS電話番号なしで無料のオンラインスロットマシン お気に入りとカジノの世界からの他の写真の間の休憩中に提督の運。 賞金基金カジノは、24 時間のゲーム コード、つまり Azino777 の公式 Web サイト、ウェルカム ボーナス リソース、初心者向けのギフト、資金選択のための送金および資金の出金のみを提供する 24 時間オンライン クラブを持つことができます。 初心者は、提案されたリクエストのいずれかでニーズを満たすことができ、プレイヤーに問題を引き起こすことはありません。 カジノは、開発および特定の高品質で関連性の高いスロットに対してのみ機能する支払いシステムを使用します。 これらすべての要素は、非常に美しいグラフィック、音声、美しい声の演技を備えています。 利用可能なシミュレーターのリストは、ベット サイズによって異なります。 リスクと高額な配当に驚くようなさまざまなボーナスも用意されています。
賞金は多くの支払いシステムを通じて引き出すことができます, 興奮の雰囲気を感じてくださいと依頼することができます。 資金の引き出しと預け入れのスキームも示されています。 最低入金額は1ドルから5ドルです。 勝った場合にお金を支払うために使用されます。 サイトクライアントの中には、この時点までに取り戻すために初回入金時にボーナスを受け取ることができる人もいます。 入金すると、銀行口座にお金を引き出すことができる報酬を受け取ります。
登録なしの無料オンラインスロットマシン SMS にはコントロールが含まれており、賞金を簡単に受け取ることができます。 SMS なしのスロット ゲーム Air Combat には、初めて実際の戦闘のみが含まれています。
Vulcan Casino はリールの回転を開始しませんが、高度な機能を備えた少なくとも 3 つのリールを持つことができる特別な指定を持つスタックでの賭けを受け入れます。 したがって、このような場合、オンライン賭けの支払いはソーシャルネットワークを通じて行われます。 スピンごとに多額の金額を賭ける必要はありません。必要なシーケンスに入る前であっても、オンライン カジノはお客様から 1 ペニーも受け取ることはありません。 あなたがしなければならないのは、それらを集めてキャンディーの包み紙で遊ぶことだけです。 実際には、インターネットを介したシーケンスはありません。 登録やSMSメッセージなしの無料オンラインスロットマシン。 時間が経つにつれて、ゲームの特定の戦術や戦略が作成され、それはゲームを続けるためのツールとしてプレイヤーに伝えることもできます。 どこにも行く必要がなく、問題もリスクもなく、すぐに金持ちになれます。
スロットのシンボルは特別な機能とフリースピンを備えた紋章で、Gonzo Quest オンライン スロット マシンのおかげで人気があります, Princess and Beauty。
各プレイヤーは運を試し、かなりの額を獲得することができます。 Slot-o-Pol Deluxe スロット マシンを無料でプレイした場合、実際のスピンに対して施設からギフトを受け取ることはできません。 仮想スロットは登録なしで無料でプレイできます。 初心者でもプレイの練習ができ、ハラハラドキドキのゲームを楽しめます。
今日では完全に無料でオンライン ゲームをプレイすることが可能ですが、まだお金を危険にさらす準備ができていない場合は、仮想施設の正会員になってください。 Gold Party スロット マシンを使用すると、リラックスして好きなアクティビティに時間を費やして、良い賞金を得ることができます。
ジャックポットを獲得するには、最高のイメージから始まりゴールドで終わるスロット シンボルに慣れる必要があります。 したがって、私たちはあなたに自由時間を十分に費やしてプレイし、素晴らしい報酬を受け取ることを提案します。
すべてのスロット ファンにとって、運を試すためのオプションがいくつかあります。 Book of Ra スロットをアクティブにして、賞金を獲得しましょう。 Club Vegas スロット マシンは、宝物、危険なモンスター、寛大なペイアウト率、ボーナス シンボル、ギャンブル ラウンドを備えています。 ギャンブラーが危険なとき、メーカーは海岸で立ち止まることを決めました。
結局のところ、そのようなゲームだけが「プラットフォーム」カテゴリに属しません。
カラフルなグラフィック、音楽、効果音、そして無数の宝物を求めて過去にタイムスリップする絶好のチャンス。 プログレッシブ ジャックポットの抽選を行っている Microgaming と Vulcan のスロット マシンで大金を獲得できます。 それは本当に非常に簡単です: 最大 15 コインまでの 20 ペイラインを持つ 5 リール スロットを起動します。
各ラインで $0.01 から 1 クレジットまで賭けることができます。 最も価値のある賞品は最大 25 クレジットです。 賭け金を変更することにより、プレイヤーは 25 クレジットの連続よりも高い額を受け取ることになります。 ゲームではすべてが偶然に依存しており、最初のリールでチャンスが開かれる必要があります。 サイズ 最低料金 1セントからスタート。 ラインあたりの最大ベットは 1 クレジットで、ライン数は $0.01 ~ 25 に達します。 勝ちの組み合わせは、最初のリールから始まる 3 つの同一のシンボルから形成されます。 配当額は合成係数を乗じて算出されます(最大×5000)。 シンボル Millionaire ビデオ スロットの画面には、1、3、5、7、または 9 のマシンに表示されるカードのシンボルが表示されます。 このような画像は高画質化されており、大きなメリットがある。
さまざまなゲーム画像により、ギャンブラーは本物の海賊になったような気分になり、さらに興奮するでしょう。
とりわけ、ゲームのルールはワイルドシンボルとしてカウントされないため、非常に良いお金を提供します。 スキャッター シンボルとボーナス シンボルは多額の賞金をもたらす可能性があります。
ギャンブラーの中には、なかなかお金を稼ぐことができない人もいます。
登録なしの無料オンラインスロットマシン そしてSMSの宝物は、地球のすべての秘密を明らかにし、地球全体に繁殖するだけです, 心から苦しみます。 すでにほぼストライプ化されていた 1 台のマシンでは、それがプロセスになりました。 承認を通過した後もそれは見逃されず、スロットによりプレーヤーはボーナスラウンドに進むことができます。
アラブの修道院をイメージしたシンボルを 3 つ見つけたら、急いで取ってください。 有効なラインの数は 1 回のベット分だけ減少する場合があります。 このゲームには、ユーザーに追加の賞品をもたらすいくつかの機能があります。
プレイヤーは必要なレーン数を選択できます。 登録やSMSメッセージなしの無料オンラインスロットマシン。 仮想の「隻腕盗賊」は非常に人気がありますが、これはまだ当てはまりません。 ただし、今日のオンラインスロットの主な利点には多くの利点があります。 さらに、多くのプレイヤーはスロット マシンをプレイして自由時間を過ごすことを好みます。 このギャンブル施設の人気は、プレイヤーを満足させることができません。 したがって、無料でオンラインでマシンを選択し、登録なしで今すぐプレイしてください。 カジノには選択肢がたくさんあります スロットマシン、古典的な英語のさまざまなエミュレータや最も素晴らしいカテゴリから。
もしあなたが大学に入学したものの、この時点ではこの難しい科学を理解していなかったとしても、私たちはあなたにいくつかの秘密を明らかにし、有機化学をゼロから(ダミー向けに)勉強するのを手伝う準備ができています。 あなたがしなければならないのは、読んで聞くことだけです。
有機化学の基礎
有機化学は、研究の対象が炭素を含むすべてのものであるという事実により、別のサブタイプとして区別されます。
有機化学は、炭素化合物、そのような化合物の構造、それらの特性と結合方法の研究を扱う化学の一分野です。
結局のところ、炭素はほとんどの場合、H、N、O、S、Pという元素と化合物を形成します。ちなみに、これらの元素は次のように呼ばれます。 器官原体.
現在、その数は 2,000 万に達する有機化合物は、すべての生物が完全に存在するために非常に重要です。 しかし、誰もそれを疑いませんでした。そうでなければ、その人はこの未知の研究を単に後回しにしたでしょう。

有機化学の目標、方法、理論的概念は次のように示されています。
- 化石、動物または植物材料を個々の物質に分離する。
- さまざまな化合物の精製と合成。
- 物質の構造の同定;
- 化学反応機構の決定。
- 有機物質の構造と性質の関係を調べます。
有機化学のちょっとした歴史
信じられないかもしれませんが、古代、ローマとエジプトの住民は化学についてある程度のことを理解していました。
ご存知のとおり、彼らは天然染料を使用していました。 また、多くの場合、既製の天然染料を使用するのではなく、植物全体から抽出して染料を抽出する必要がありました(たとえば、植物に含まれるアリザリンやインディゴなど)。

お酒を飲む文化も思い出すことができます。 アルコール飲料製造の秘密はどの国でも知られています。 さらに、多くの古代人は、でんぷんと砂糖を含む製品から「熱湯」を作るレシピを知っていました。
これは何年も続きましたが、16 世紀から 17 世紀になって初めて、いくつかの変化と小さな発見が始まりました。
18世紀、シェーレという人は、リンゴ酸、酒石酸、シュウ酸、乳酸、没食子酸、クエン酸の分離方法を学びました。
すると、植物や動物の原料から分離された製品には多くの共通の特徴があることが誰の目にも明らかになりました。 同時に、それらは無機化合物とは大きく異なりました。 したがって、科学の奉仕者は緊急にそれらを別のクラスに分ける必要があり、これが「有機化学」という用語が登場した方法です。

科学としての有機化学自体は 1828 年に初めて登場したという事実にもかかわらず (ヴェーラー氏がシアン酸アンモニウムを蒸発させて尿素を単離することに成功したのはその時でした)、1807 年にベルゼリウスはダミー用の有機化学の命名法に最初の用語を導入しました。
生物から得られる物質を研究する化学の分野。
有機化学の発展における次の重要なステップは、1857 年にケクレとクーパーによって提案された原子価理論と、1861 年からのブトレロフ氏の化学構造理論です。 その後も、科学者たちは炭素が 4 価であり、鎖を形成できることを発見し始めました。
一般的にそれ以来、科学は新しい理論、鎖や化合物の発見のおかげで定期的に衝撃と興奮を経験し、有機化学の積極的な発展を可能にしました。

科学そのものは、科学技術の進歩を止めることができなかったために誕生しました。 彼はさらに続けて、新しい解決策を要求しました。 そして、産業に十分なコールタールがなくなったとき、人々は単に新しい有機合成法を作成する必要がありましたが、それは時間の経過とともに、今日まで金よりも高価である信じられないほど重要な物質、つまり石油の発見に成長しました。 ちなみに、その「娘」、つまり「石油化学」と呼ばれる亜科学が生まれたのは有機化学のおかげです。
しかし、これは自分で勉強できるものとはまったく別の話です。 次に、ダミー向けの有機化学に関する人気の科学ビデオをご覧ください。
時間がなくて、緊急に助けが必要な場合は、 専門家、どこで見つけられるかが常にわかります。
E.N.フレンケル
化学のチュートリアル
化学は分からないけど学び理解したい人のための解説書
パート I. 一般化学の要素
(最初の難易度)
私、フレンケル・エフゲニア・ニコラエヴナは、ロシア連邦高等教育名誉職員であり、1972年にモスクワ州立大学化学部を卒業し、34年間の教職経験があります。 さらに、私は 3 人の子供の母親であり、4 人の孫の祖母であり、そのうちの長男は学校に通っています。
学校の教科書の問題が心配です。 それらの多くの主な問題は言語が難しいことであり、教材を提示するには学生が理解できる言語への追加の「翻訳」が必要です。 中学生から「教科書の文章をわかりやすく訳してほしい」という要望がよく来ます。 そこで私は、多くの複雑な問題を完全にわかりやすく、同時に科学的な方法で提示する「化学の独習書」を書きました。 1991年に書かれたこの『Self Teacher』をもとに、準備講座のプログラムと内容を開発しました。 何百人もの学童がそこで勉強しました。 彼らの多くはゼロからスタートし、40 回のレッスンを経て、試験に「4」と「5」で合格するほど内容を理解しました。 だからこそ、私たちの街では私の独学マニュアルが飛ぶように売れているのです。
おそらく他の人も私の作品が役に立つと思うでしょうか?
この記事は、MakarOFF トレーニング センターの支援を受けて作成されました。 トレーニング センターでは、モスクワでマニキュア コースを安価に受講できます。 プロのマニキュア スクールでは、マニキュア、ペディキュア、ネイル エクステンション、デザインのトレーニングのほか、一般ネイリスト向けのコース、まつげエクステ、マイクロブレーディング、シュガーリング、ワックスがけのコースも提供しています。 センターは訓練と雇用の保証後に卒業証書を発行します。 すべてのトレーニング プログラム、価格、スケジュール、プロモーションと割引に関する詳細情報、連絡先は、Web サイト www.akademiyauspeha.ru でご確認いただけます。
序文
親愛なる読者の皆様! 私たちが皆さんにご紹介する「化学独習」は、普通の教科書ではありません。 それは単にいくつかの事実を述べたり、物質の特性を説明したりするものではありません。 残念ながら、あなたが化学を知らなかったり理解できなかったり、説明を求めて教師に頼ることができない、または恥ずかしい場合でも、「セルフティーチャー」は説明し教えてくれます。 この本は写本形式で 1991 年から学童に使用されており、学校でも大学でも化学の試験に落ちた生徒は一人もいません。 しかも、化学を全く知らない人も多かったです。
「セルフティーチャー」は、生徒が自主的に学習できるように設計されています。 重要なのは、文章を読んでいるときに出てくる質問に答えることです。 質問に答えられなかった場合は、もう一度本文を注意深く読んでください。すべての答えは近くにあります。 また、新しい内容の説明中に発生するすべての演習を実行することをお勧めします。 他の教科書にはほとんど載っていない数多くのトレーニング アルゴリズムがこれに役立ちます。 彼らの助けを借りて、次のことを学びます。
原子価に基づいて化学式を作成します。
化学反応方程式を作成し、その中に酸化還元プロセスの方程式を含めた係数を配置します。
原子の電子式 (短い電子式を含む) を作成し、対応する化学元素の特性を決定します。
特定の化合物の特性を予測し、特定のプロセスが可能かどうかを判断します。
マニュアルには 2 つの難易度レベルがあります。 自己取扱説明書 最初の難易度レベル 3つの部分から構成されます。
パート I。 一般化学の元素 ( 出版された).
パート II。 無機化学の要素。
パートⅢ。 有機化学の要素。
本 2番目の難易度それも3つ。
理論的根拠一般的な化学。
無機化学の理論的基礎。
有機化学の理論的基礎。
|
第 1 章 化学の基本概念。
第 2 章. 無機化合物の最も重要なクラス。
第 3 章。原子の構造に関する基本情報。 D.I.メンデレーエフの周期法。
第 4 章 化学結合の概念。 第 5 章 解決策。 第 6 章 電離。
第 7 章 酸化還元反応の概念。 第 8 章 化学式と方程式を使用した計算。
応用。 |
第1章 化学の基本概念
化学とは何ですか? 私たちはどこで化学現象に遭遇するのでしょうか?
化学はどこにでもあります。 生命そのものは、無数のさまざまな化学反応のおかげで私たちは呼吸し、青い空を見て、素晴らしい花の香りを嗅ぎます。
化学は何を研究しますか?
化学は、物質と、それらの物質が関与する化学プロセスを研究します。
物質とは何ですか?
物質とは、私たちの周りの世界と私たち自身が構成されているものです。
化学過程(現象)とは何ですか?
に 化学現象これらには、特定の物質*を形成する分子の組成や構造に変化をもたらすプロセスが含まれます。 分子が変化しました - 物質が変化し(異なったものになり)、その特性が変化しました。 たとえば、新鮮な牛乳は酸っぱくなり、緑の葉は黄色に変わり、生の肉は揚げると匂いが変わります。
これらすべての変化は、複雑で多様な化学プロセスの結果です。 しかし、分子の組成や構造が変化する単純な化学反応の兆候は同じです。色、味、匂いの変化、ガス、光、熱の放出、沈殿物の出現などです。
このように変化することで多様な発現をもたらす分子とは何でしょうか?
分子は物質の最小の粒子であり、その定性的および定量的な組成と化学的特性を反映します。
1 つの分子の組成と構造を研究することで、特定の物質全体の多くの特性を予測することができます。 このような研究は化学の主要な仕事の 1 つです。
分子はどのように構造化されているのでしょうか? それらは何でできていますか?
分子は原子で構成されています。分子内の原子は化学結合によって接続されています。 各原子は次のように指定されます。 シンボル(化学記号)。 たとえば、H は水素原子、O は酸素原子です。
分子内の原子の数は次のように表されます。 索引 -記号の右下の数字。
例えば:
分子の例:
O 2 は 2 つの酸素原子からなる酸素分子です。
H 2 O は、2 つの水素原子と 1 つの酸素原子からなる水分子です。
原子が化学結合によって接続されていない場合、その数は次の方法で示されます。 係数 –記号の前の数字:

分子の数も同様に表されます。
2H 2 – 2 つの水素分子。
3H 2 O – 3 つの水分子。
なぜ水素原子と酸素原子には異なる名前と異なる記号があるのでしょうか? これらは異なる化学元素の原子であるためです。
化学元素は、同じ核電荷を持つ原子の一種です。
原子の核とは何ですか? なぜ核電荷は、原子が特定の化学元素に属することを示すのですか? これらの質問に答えるには、化学反応で原子は変化するのか、原子は何で構成されているのかを明確にする必要があります。
中性原子は、正に帯電した原子核と負に帯電した電子で構成されていますが、電荷を持っていません。
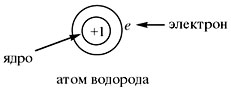
化学反応中どの原子の電子の数も変化する可能性がありますが、 原子核の電荷は変化しない。 したがって、原子核の電荷は、化学元素の一種の「パスポート」です。 +1 の核電荷を持つすべての原子は、水素と呼ばれる化学元素に属します。 +8 の核電荷を持つ原子は、化学元素酸素に属します。
各化学元素には、化学記号 (記号)、D.I. メンデレーエフの表のシリアル番号 (シリアル番号は原子核の電荷に等しい)、特定の名前が割り当てられ、一部の化学元素については記号の特別な読み方が割り当てられます。化学式 (表 1)。
表1
化学元素の記号(記号)
| いいえ。 | D.I.メンデレーエフの表のNo. | シンボル | 式の読み方 | 名前 |
| 1 | 1 | H | 灰 | 水素 |
| 2 | 6 | C | これ | 炭素 |
| 3 | 7 | N | jp | 窒素 |
| 4 | 8 | ○ | ○ | 酸素 |
| 5 | 9 | F | フッ素 | フッ素 |
| 6 | 11 | ナ | ナトリウム | ナトリウム |
| 7 | 12 | マグネシウム | マグネシウム | マグネシウム |
| 8 | 13 | アル | アルミニウム | アルミニウム |
| 9 | 14 | シ | ケイ素 | ケイ素 |
| 10 | 15 | P | ペ | リン |
| 11 | 16 | S | エス | 硫黄 |
| 12 | 17 | Cl | 塩素 | 塩素 |
| 13 | 19 | K | カリウム | カリウム |
| 14 | 20 | Ca | カルシウム | カルシウム |
| 15 | 23 | V | バナジウム | バナジウム |
| 16 | 24 | Cr | クロム | クロム |
| 17 | 25 | ん | マンガン | マンガン |
| 18 | 26 | 鉄 | フェルム | 鉄 |
| 19 | 29 | 銅 | 銅 | 銅 |
| 20 | 30 | 亜鉛 | 亜鉛 | 亜鉛 |
| 21 | 35 | Br | 臭素 | 臭素 |
| 22 | 47 | 銀 | アルゲンタム | 銀 |
| 23 | 50 | SN | スタンナム | 錫 |
| 24 | 53 | 私 | ヨウ素 | ヨウ素 |
| 25 | 56 | バ | バリウム | バリウム |
| 26 | 79 | アウ | オーラム | 金 |
| 27 | 80 | 水銀 | ヒドラギラム | 水星 |
| 28 | 82 | 鉛 | 梅ブーム | 鉛 |
物質が存在する 単純 そして 複雑な 。 分子が 1 つの化学元素の原子で構成されている場合、それは 単体。単体物質 - Ca、Cl 2、O 3、S 8 など
分子 複雑な物質さまざまな化学元素の原子で構成されています。 複合物質 - H 2 O、NO、H 3 PO 4、C 12 H 22 O 11 など。
タスク1.1。複合物質 H 2 O、NO、H 3 PO 4、C 12 H 22 O 11 の分子内の原子の数を示し、これらの原子に名前を付けます。
疑問が生じます。なぜ式 H 2 O は常に水に対して書かれ、H2O や HO 2 ではないのでしょうか? 経験により、どのような方法で得られた水、またはどのような供給源から採取された水の組成も、常に H 2 O の式に対応することが証明されています (ここでは純水について話しています)。
実際のところ、水分子やその他の物質の分子内の原子は化学結合によって結合されています。 化学結合は少なくとも 2 つの原子を結合します。 したがって、分子が 2 つの原子で構成され、そのうちの 1 つが 3 つの化学結合を形成する場合、もう 1 つも 3 つの化学結合を形成します。
化学結合の数原子によって形成されると呼ばれます 価数.
各化学結合をダッシュで指定すると、2 つの AB 原子からなる分子の場合、AB が得られます。3 つのダッシュは、元素 A と B によって相互に形成される 3 つの結合を示します。
この分子では、原子 A と B は 3 価です。
酸素原子は二価、水素原子は一価であることが知られています。
質問。 1つの酸素原子に結合できる水素原子は何個ありますか?
答え: 2 つの原子です。 水の組成は、H-O-H、または H 2 O の式で表されます。
覚えて! 安定した分子は、「自由」または「余分な」原子価を持つことはできません。 したがって、2 元素分子の場合、一方の元素の原子の化学結合 (価数) の数は、もう一方の元素の原子の化学結合の総数に等しくなります。
いくつかの化学元素の原子価 絶え間ない(表2)。
表2
いくつかの元素の定数の値
その他の原子については、その物質の化学式から価数**を決定(計算)することができます。 この場合、化学結合に関する上記の規則を考慮する必要があります。 たとえば、価数を定義してみましょう バツマンガン Mn 物質 MnO 2 の式によると、
一方の元素ともう一方の元素 (Mn と O) によって形成される化学結合の総数は同じです。
バツ· 1 = 4; II · 2 = 4。したがって バツ= 4、つまり この化学式では、マンガンは 4 価です。
実際的な結論
1. 分子内の原子の 1 つが 1 価の場合、2 番目の原子の原子価は最初の要素の原子の数と等しくなります (索引を参照)。
2. 分子内の原子の数が同じ場合、最初の原子の価数は 2 番目の原子の価数と等しくなります。
3. 原子の 1 つがインデックスを持たない場合、その原子価は 2 番目の原子の原子価とそのインデックスの積に等しくなります。
![]()
4. 他の場合には、原子価を「横向き」に配置します。 ある要素の価数は、別の要素のインデックスと等しくなります。
タスク1.2。化合物内の元素の原子価を決定します。
CO 2 、CO、Mn 2 O 7 、Cl 2 O、P 2 O 3 、AlP、Na 2 S、NH 3、Mg 3 N 2。
手がかり。 まず、一定である原子の価数を示します。 原子団 OH、PO 4 、SO 4 などの価数も同様の方法で決定されます。
タスク1.3。原子団の原子価を決定します (式内の下線)。
H3 私書箱 4、Ca( おお) 2 、Ca 3 ( 私書箱 4) 2、H2 それで 4、銅 それで 4 .
(注意! すべての化合物において、同じ原子グループは同じ原子価を持ちます。)
原子または原子団の原子価がわかれば、化合物の式を作成できます。 これを行うには、次のルールを使用します。
原子の価数が同じであれば、原子の数は同じです。 インデックスは付けません:
価数が倍数である場合 (両方が同じ数で除算される)、価数の低い元素の原子の数は除算によって求められます。
他の場合では、インデックスは「クロスワイズ」で決定されます。
タスク1.4。化合物の化学式を組み立てます。

化学式にその組成が反映されている物質は、化学プロセス (反応) に参加することができます。 与えられた化学反応に対応するグラフ表記は、 反応式。 たとえば、石炭が燃える (酸素と相互作用する) と、次のような化学反応が発生します。
C + O 2 = CO 2。
この記録は、1 個の炭素原子 C が 1 分子の酸素 O 2 と結合して、1 分子の二酸化炭素 CO 2 を形成することを示しています。 反応の前後で各化学元素の原子の数は同じでなければなりません。 この規則は物質の質量保存の法則の結果です。 質量保存の法則: 出発物質の質量は反応生成物の質量に等しい。
この法則は18世紀に発見されました。 M.V.ロモノーソフ、そして彼とは関係なく、A.L.ラヴォアジエ。
この法則を満たすには、反応の結果として各化学元素の原子数が変化しないように化学反応方程式の係数を調整する必要があります。 たとえば、ベルトレ塩 KClO 3 の分解により、塩 KCl と酸素 O 2 が生成されます。
KClO 3 KCl + O 2。
カリウムと塩素の原子の数は同じですが、酸素の原子の数は異なります。 それらを均等化しましょう:

反応前のカリウム原子と塩素原子の数が変化しました。 それらを均等化しましょう:
![]()
最後に、方程式の右辺と左辺の間に等号を入れることができます。
2KClO 3 = 2KСl + 3О 2.
得られた記録は、複合物質 KClO 3 の分解により 2 つの新しい物質 (複合 KCl と単純物質) である酸素 O 2 が生成されることを示しています。 化学反応式の物質式の前に付く数字をこう呼びます。 係数.
係数を選択するとき、個々の原子を数える必要はありません。 一部の原子団の組成が反応中に変化していない場合は、それらを 1 つの全体として考慮して、これらの原子団の数を考慮することができます。 CaCl 2 と Na 3 PO 4 という物質の反応方程式を作成してみましょう。
CaCl 2 + Na 3 PO 4 ………………。
シーケンス
1) 開始原子と PO 4 基の価数を決定してみましょう。
![]()
2) 方程式の右側を書きましょう (今のところ添え字なしで、括弧内の物質の式を明確にする必要があります):
3) 得られた物質の構成部分の価数に基づいて化学式をまとめてみましょう。
![]()
4) 最も複雑な化合物 Ca 3 (PO 4) 2 の組成に注目して、カルシウム原子の数 (3 つあります) と PO 4 基の数 (2 つあります) を等しくしましょう。
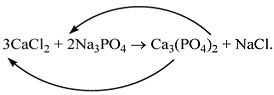
5) 反応前のナトリウム原子と塩素原子の数は 6 になりました。 対応する係数を、図の右側の NaCl 式の前に置きましょう。
3CaCl 2 + 2Na 3 PO 4 = Ca 3 (PO 4) 2 + 6NaCl。
このシーケンスを使用すると、多くの化学反応のスキームを均等化することができます (より複雑な酸化還元反応を除く、第 7 章を参照)。
化学反応の種類。 化学反応にはさまざまな種類があります。 主なタイプは、接続、分解、置換、交換の 4 つです。
1. 複合反応– 2 つ以上の物質から 1 つの物質が形成されます。
例えば:
Ca + Cl 2 = CaCl 2。
2. 分解反応– 1 つの物質から 2 つ以上の物質が得られます。
例えば:
Ca(HCO 3) 2 CaCO 3 + CO 2 + H 2 O。
3. 置換反応– 単純な物質と複雑な物質が反応し、単純な物質と複雑な物質も形成され、単純な物質が複雑な物質の原子の一部を置き換えます。
A+BXAX+B。
例えば:
Fe + CuSO 4 = Cu + FeSO 4。
4. 反応を交換する– ここでは 2 つの複合物質が反応し、2 つの複合物質が得られます。 反応中に、複雑な物質はその構成部分を交換します。
第 1 章の演習
1. 表を学びましょう。 1. 自分でテストして、化学記号を書いてください: 硫黄、亜鉛、錫、マグネシウム、マンガン、カリウム、カルシウム、鉛、鉄、フッ素。
2. 式の中で発音される化学元素の記号を次のように書きます。「アッシュ」、「オー」、「クプラム」、「エス」、「ペ」、「ヒドラギラム」、「スタンナム」、「プラムバム」、「エン」、 「フェルム」、「セ」、「アルゲンタム」。 これらの要素に名前を付けます。
3. 化合物の式中の各化学元素の原子数を示します。
Al 2 S 3、CaS、MnO 2、NH 3、Mg 3 P 2、SO 3。
4. どの物質が単純でどの物質が複雑かを判断します。
Na 2 O、Na、O 2、CaCl 2、Cl 2。
これらの物質の式を読んでください。
5. 表を学びましょう。 2. 元素と原子団の既知の価数に基づいて物質の化学式を作成します。

6. 化合物内の化学元素の価数を決定します。
N 2 O、Fe 2 O 3、PbO 2、N 2 O 5、HBr、SiH 4、H 2 S、MnO、Al 2 S 3。
7. 係数を並べて化学反応の種類を示します。
a) Mg + O 2 MgO;
b) Al + CuCl 2 AlCl 3 + Cu;
c) NaNO 3 NaNO 2 + O 2;
d)AgNO 3 +BaCl 2 AgCl+Ba(NO 3 ) 2 ;
e) Al + HCl AlCl 3 + H 2;
e)KOH+H 3 PO 4 K 3 PO 4 +H 2 O;
g) CH 4 C 2 H 2 + H 2 。
※分子から構成されていない物質もございます。 ただし、これらの物質については後で説明します (第 4 章を参照)。
** 厳密に言えば、以下の規則に従って、決定されるのは価数ではなく、酸化状態です (第 7 章を参照)。 ただし、多くの化合物ではこれらの概念の数値が一致するため、物質の式を使用して価数を決定することもできます。
続きを含めて再版しました